May.07.2026
分類主題:研究報告適用範圍:
作者:Nüs Hisim,Vernier 化學教育科技專家

如果您在 AP 化學或大學普通化學中教過化學平衡,您一定知道這個經典的實驗設定:將酸加入指示劑中,觀察其顏色變化,然後加入鹼,觀察它變回原來的顏色。這個實驗設定很好地說明了勒沙特列原理 (Le Chatelier's principle)——但它卻止步於真正化學反應發生的地方。如果學生能實際從顏色變化中計算出平衡常數呢?
這正是這個實驗所要做的。使用溴百里酚藍 (BTB)、一個 Go Direct® pH 感應器,以及一台 Go Direct SpectroVis® Plus 光譜儀,學生測量平衡時兩種指示劑形式的濃度,並使用比爾定律 (Beer's law) 求出 Keq 的真實值。
結果是這將成為一個更具定量嚴謹性的實驗——同時也是一個更安全、更環保的實驗。
如果你做過經典的硫氰酸鐵 (iron(III) thiocyanate) 平衡實驗,你一定知道流程:硝酸鐵、硝酸、危險的 SDS 表格,以及你絕對不應該倒入排水管的化學物質。它有效,但安全和廢棄物處理的擔憂是真實存在的。
溴百里酚藍解決了這個問題。指示劑本身和用於轉移平衡的磷酸氫鈉溶液是無害的——處理起來很安全,而且可以安全地與水一起倒入排水管中。唯一需要額外小心的化學物質是用於比爾定律部分的 0.1 M HCl 和 NaOH,但在這種濃度下,它們很溫和。
除了更安全的化學物質外,這個實驗還體現了其他幾個綠色化學原則:
學生甚至在實驗後會直接對此進行反思,這使得綠色化學的角度成為真正的學習成果,而不僅僅是一個註腳。
溴百里酚藍是一種弱酸指示劑,根據 pH 值的不同,以兩種形式存在:
HIn + H2O ⇄ In– + H3O+

那個綠色區域就是奇蹟發生的地方。當兩種成分都對吸光度產生有意義的貢獻時,您可以使用分光光度法獨立測量每一種成分——這就是計算 Keq 成為可能的原因。
這是學生需要求解的平衡表達式:
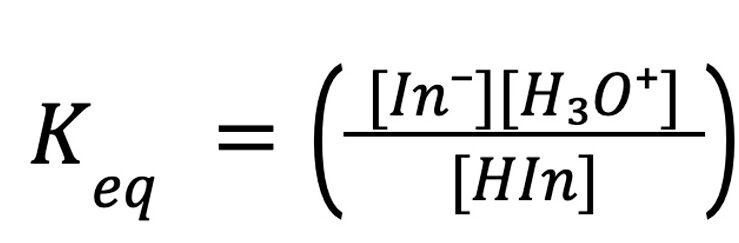
要找到它,學生需要三個數值:

關於 BTB 的注意事項: 儲備的 BTB 通常為 0.04% 溶液。實驗前的其中一項任務是將其轉換為莫耳濃度 (molarity)——這是一個很好的提醒,百分比濃度和莫耳濃度是不一樣的。
關於蒸餾水的注意事項: 使用新鮮的蒸餾水。暴露在空氣中的蒸餾水會吸收 CO₂,導致 pH 值下降,並在你開始做任何事情之前就使你的 BTB 變成黃色。如果你的 BTB 在蒸餾水中看起來是黃色的而不是綠色的,這通常是原因。
在進行任何定量工作之前,學生會花時間觀察 BTB 如何響應 pH 值的變化。
他們將少量的稀酸和稀鹼加入 BTB 溶液中,並捕捉每一步的吸收光譜,觀察顏色和光譜的變化。
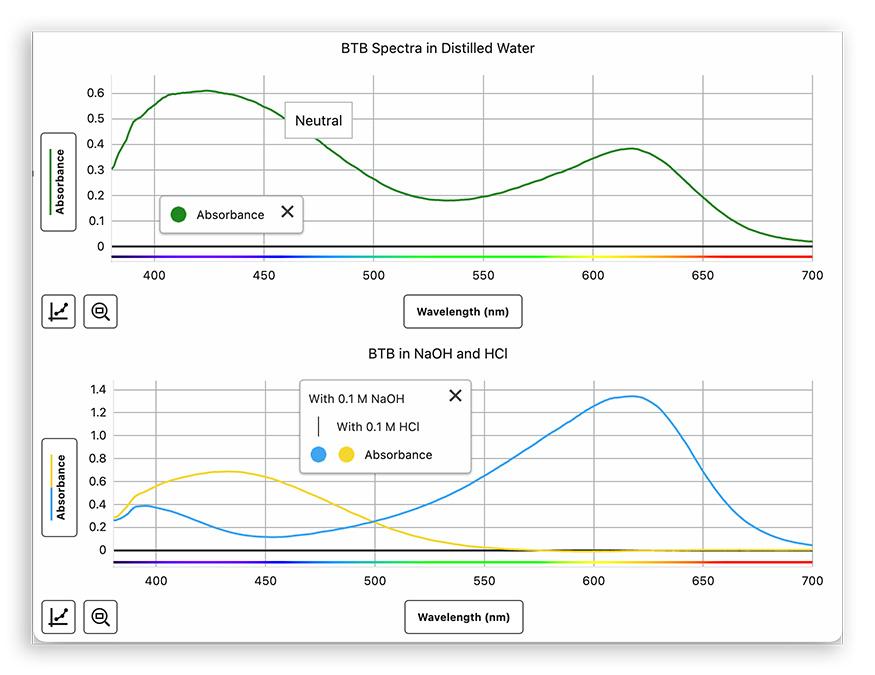 中性、低 pH 值和高 pH 值下溴百里酚藍的吸收光譜
中性、低 pH 值和高 pH 值下溴百里酚藍的吸收光譜目標是確定兩個峰值波長——一個對應指示劑的每一種形式——這將為接下來的所有工作奠定基礎。
這也是在定量工作開始之前,讓學生熟悉 Spectral Analysis 應用程式的一種低風險方式。
接下來,學生準備一組已知濃度的溴百里酚藍溶液——一種呈酸性(黃色),另一種呈鹼性(藍色)。
然後,他們繪製吸光度與濃度的關係圖,以確定每個峰值波長處的莫耳吸光係數 (molar absorptivity, ε)。每條線性圖的斜率即為 ε,也就是他們在第二部分中計算未知濃度所需的比例常數。
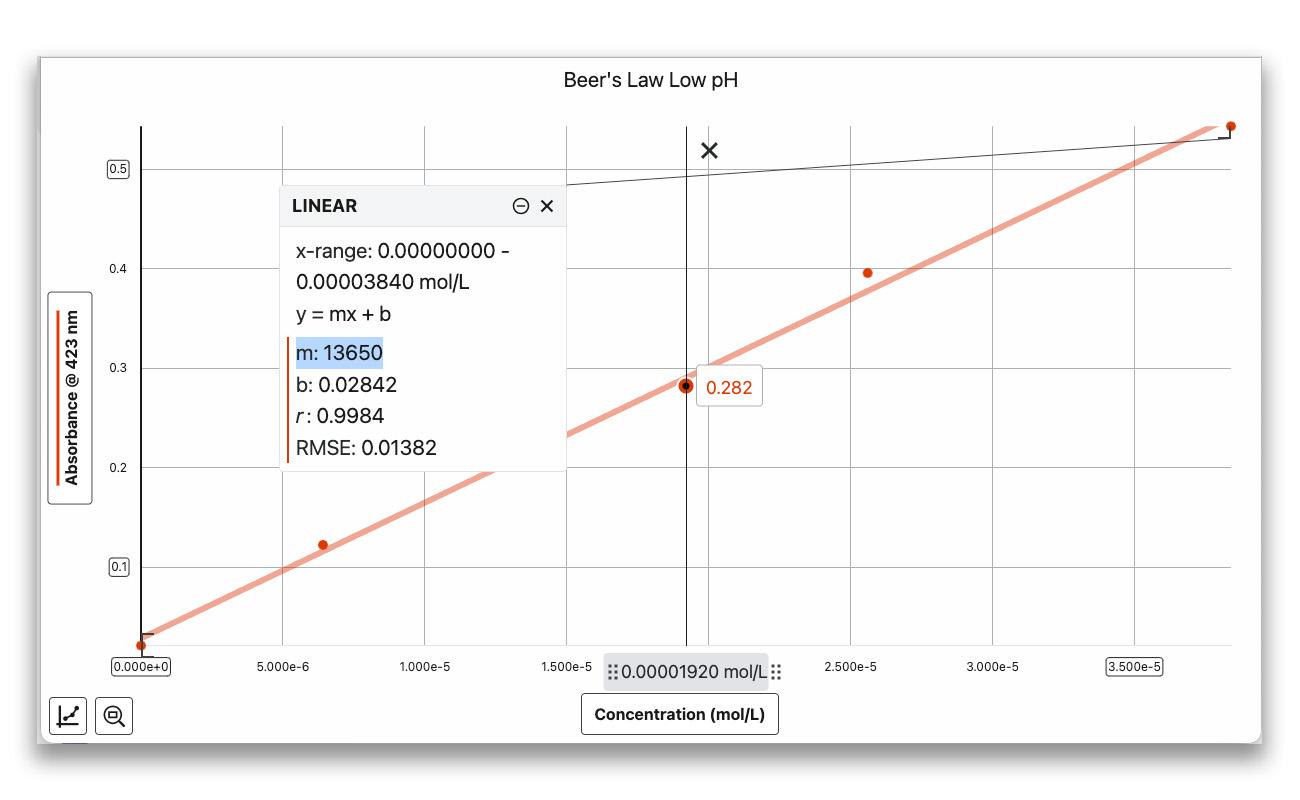 低 pH 值組
低 pH 值組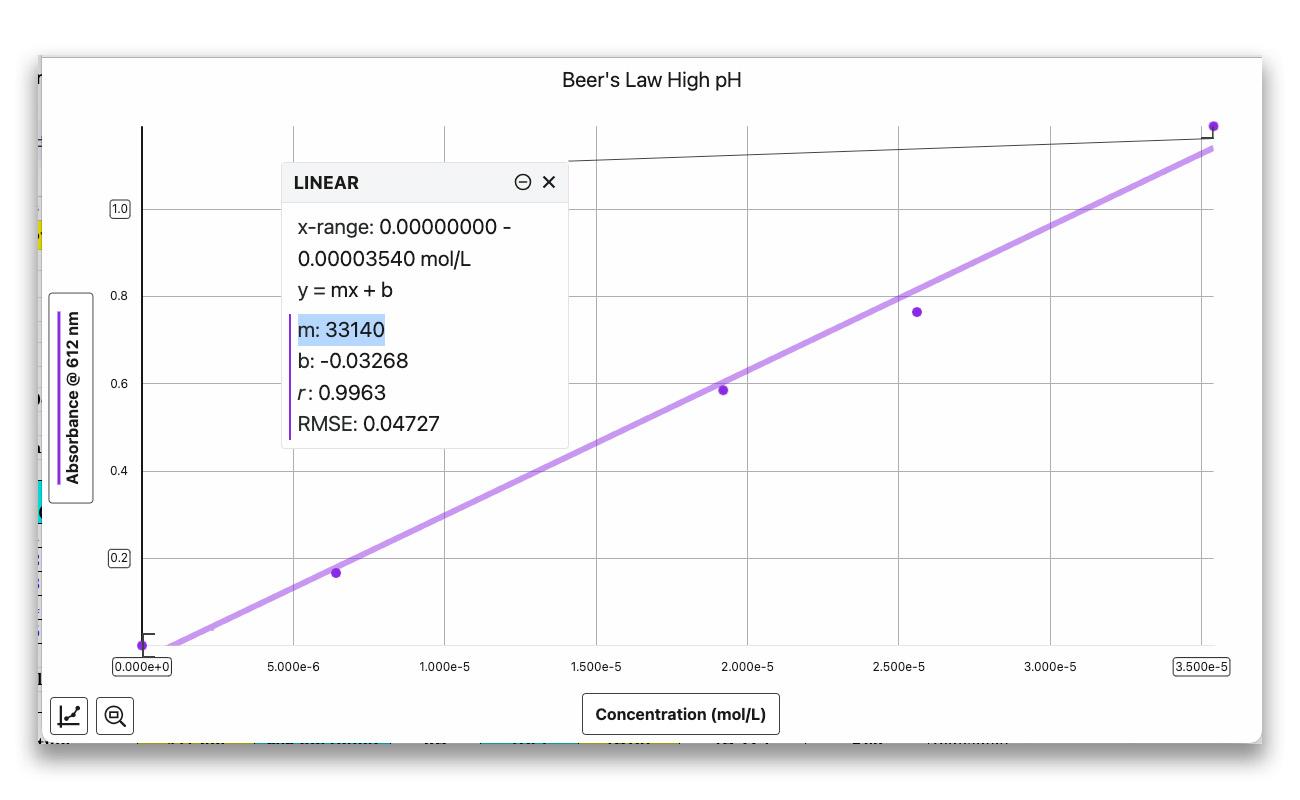 高 pH 值組
高 pH 值組使用線性曲線擬合每個圖表。這條線的斜率是 ε,莫耳吸光係數。
實用技巧: 將吸光度值保持在 1.0 以下,以獲得可靠的比爾定律數據。如果溶液超過此值,請將其稀釋至已知濃度並重新測量。
有了比爾定律圖後,學生準備三種 BTB 溶液,並使用磷酸氫鈉(溫和、安全的試劑)將每種溶液轉移到略微不同的 pH 值,這能輕輕推動平衡而不會過度反應。
目標範圍是 pH 6-7,在此範圍內,BTB 的兩種形式都以可測量的數量存在。
對於每種溶液,學生測量:
結合 pH 值和吸光度數據,這就是他們求解 Keq 所需的一切。
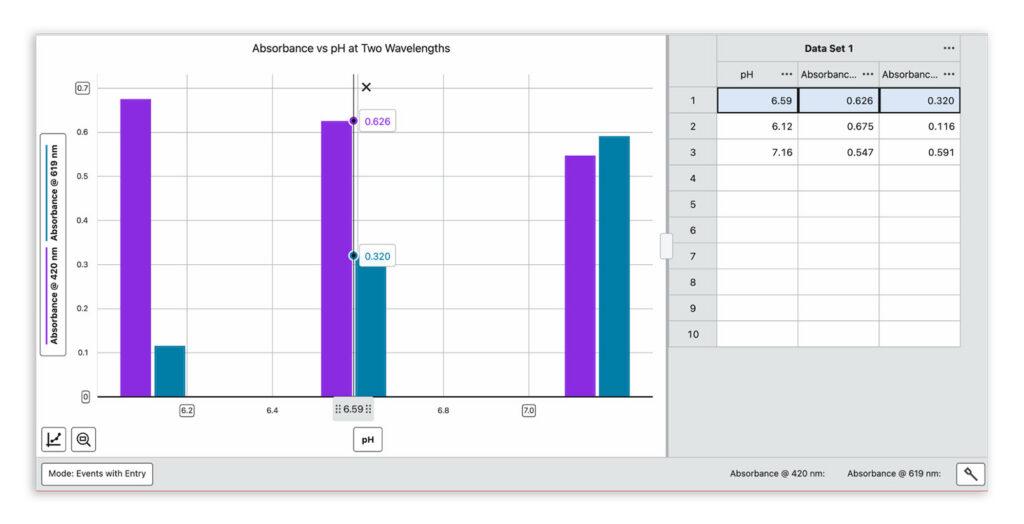
使用比爾定律圖中的莫耳吸光係數,學生根據吸光度數據計算 HIn 和 In⁻ 的濃度。
水合氫離子的濃度由測量到的 pH 值確定。
將這些值代入平衡表達式,即可得出 Keq 的值。
如果您在教 AP 化學,這是一個自然連結到 ICE 表格和平衡表達式的地方。學生不僅是在觀察平衡的轉移——他們正在量化它。
這個實驗為學生提供了持續的練習,讓他們規劃並執行調查、分析和解釋數據,並使用數學和運算思維來建構解釋。
實驗後的討論包含一個專門的問題,要求學生透過綠色化學的視角評估實驗:減少廢棄物、更安全的溶劑、能源效率和適當的處置。這是一個很好的討論起點,學生通常會浮現出比您預期更多的關聯性。
